Hepatitt C-virus
Opprydding: Denne artikkelen kan ha godt av ei opprydding. Sjå korleis du redigerer ei side og stilmanualen for hjelp. |
| Hepatitt C-virus | |
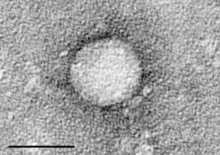 Hepatitt C-virus | |
| Systematikk | |
| Familie: | Flaviviridae |
| Slekt: | Hepacivirus |
| Art: | Hepatitt C-virus H. C |
| Vitskapleg namn | |
| Hepatitis C virus | |

Hepatitt C-virus (HCV) er årsak til ein viral leverinfeksjon kalla hepatitt C.
Klassifisering[endre | endre wikiteksten]
HCV er eit RNA-virus med ein storleik på 55–65 nm. Det har kappe (som stammar frå vertcella) og eit ikosaederforma skjelett der glykoprotein E1 og E2 er festa til eit dobbelt lipidlag i kappa. Inne i kappa finst nukleokapsidet som er samansett av mange kopiar av core-proteinet og rommar den positivt ladde RNA-strengen i genomet.
HCV er det einaste sjukdomsframkallande viruset i slekta Hepacivirus i familien Flaviviridae (i same familien er dessutan virus som framkallar denguefeber, gul feber og skogflåttencefalitt (TBE).
Dei fleste RNA-virus brukar gjeva akutte infeksjonar, men hepatitt C er som oftast ein kronisk og livslang sjukdom. Mennesket er den einaste naturlege verten for HCV. Tidlegare har det ikkje vore mogeleg å granska HCV elektronmikroskopisk eller isolera det i cellekultur.
Dette har vore eit stort hinder for all forsking. På seinare tid har molekylærbiologisk teknikk i kombinasjon med kompliserte reiningsmetodar har ført til viktige framsteg på dette området.[1] [2] [3] [4][5]

Genom[endre | endre wikiteksten]
Hjå HCV er genomet ein positivt lada RNA-streng . I kvar ende sit ein utranslert region (5´UTR og 3´UTR), den eine på 341 og den andre på 225 nukleotid. Mellom desse utranslerte regionane ligg ei open leseramme på mellom 9024 to 9111 nukleotid (ulikt for ulike genotypar). Frå denne opne leseramma kan eitt polyprotein på drygt 3000 aminosyrer avlesast. Sidan kløyver og skapar cellulære og virale proteasar om desse til strukturelle og ikkje strukturelle, regulerande protein. Dei ulike lutene utav genomet kodar for til saman minst 11 ulike preprotein: for 3 ulike strukturelle (structural) preprotein (C/core, E1/envelope og E2), for p7 som har ein noko uviss funksjon og for ytterlegare 6 ikkje strukturelle (non structural/NS) preprotein (NS2, NS3, NS4A, NS4B, NS5A og NS5B). Nokre utav desse er måltavle ved antiviral behandling av hepatitt C.
Som resultat utav ei endring i den luten av leseramma som kodar for core-regionen finst dessutan eit «F (frame shift)-protein».
5´UTR er det mest konserverte området på genomet og kodar ikkje for protein. Utan nokon translert startfaktor kan det bindast direkte til ei viss ribosomal subeining og såleis spela ei avgjerande rolle når translasjonen skal startast.
3´UTR kodar heller ikkje for protein. Det interagerer med tilgrensande område på NS5B og er viktig ved [[Avskriving i genetikk|replikasjon] av viralt RNA.
F-proteinet har ein uklar funksjon, men det ser ut til å kunna framkalla eit serologisk immunsvar ved kronisk hepatitt C. Kan henda er det involvert ved persisterande infeksjonar.
Strukturelle protein[endre | endre wikiteksten]
C (core) er viktig for oppbygging av viruskapsidet.
E1 og E2 er glykoprotein. Dei er viktige ved oppbygging av viruskappa. Ved infeksjon er fyrst og fremst E2 naudsynt av di det verkar som reseptorbindande protein når virus skal få feste og trengja inn i vertcellene.
Ikkje-strukturelle protein[endre | endre wikiteksten]
P7 er eit lite polyprotein. Det er eit viroporin som kan endra membranpermeabiliteten og verka som kanal for kalsiumion. P7 kan truleg vera viktig ved intercellulær overføring av virus i levervev.
NS2 er eit uglykosylert transmembranprotein og dannar saman med tilgrensande region på NS3 ei metallprotease som kløyver seg sjølv (autoprotease) og har stutt levetid.
NS3 er eit protein med fleire funksjonar, mellom anna som serinprotease og helikase (som hjelper til med å opna tvinningane i dobbeltspiralane ved replikasjon). NS3 er saman med ein kofaktor frå
NS4A dessutan ei særs viktig protease som katalyserer kløyving av bindingane ved NS3/NS4A, NS4A/NS4B, NS4B/NS5A og NS5A/NS5B og ofte er måltale for antivirale lækjemiddel.
NS4B er eit integrerande membranprotein som mellom anna kan tena som membrananker ved virusreplikasjon.
NS5A er eit metallprotein som truleg er viktig ved virusreplikasjon ved gripa inn i dei cellulære infeksjonsmekanismane. Binding til ein antiviral interferoneffektor kan medverka til utvikling av resistens mot interferon.
NS5B dannar ei RNA-avhengig RNA-polymerase som katalyserer syntesen av genomstrengen og difor er særs viktig ved replikasjonen av eit RNA-virus som HCV. [1]
Genotypar[endre | endre wikiteksten]
Genetiske skilnader gjer at hepatitt C-virus kan skiftast i minst 6 ulike genotypar (kjenneteikna med arabiske tal: 1,2,3 osv). Ulike område på virusgenomet syner ulike variasjonsgradar. På det fullstendige genomet ligg skilnaden mellom dei ulike genotypane i gjennomsnitt på mellom 30 og 35 % . Kvar genotype har fleire undertypar eller subgenotypar (kjenneteikna med små bokstaver (minuskel): a,b,c osv). I gjennomsnitt er det 20 – 25 % skilnad mellom nukleotidsekvensane hjå dei ulike subgenotypane. Nokre genotypar syner enda større skilnad mellom ulike subgenotypar, men det ser no ut til å råda semje om at ytterligare genotypar ikkje skal innførast. I staden skal såvorne typar oppfattast som variantar av genotypar som er kjende frå tidlegare. [3] [6]
Døme på jamførande analyse av HCV-subgenotypar[7]
(frå eit nukleotid segment på 222 sekvensar (posisjon 7975 til 8196) i NS5-regionen)
| Subgeno-
typar |
1a | 1b | 1c | 2a | 2b | 2c | 3a | 3b | 4a | 5a | 6a |
|---|---|---|---|---|---|---|---|---|---|---|---|
| 1a | 100 | 81 | 85 | 65 | 66 | 63 | 67 | 66 | 68 | 69 | 64 |
| 1b | 100 | 77 | 64 | 67 | 64 | 67 | 71 | 64 | 70 | 65 | |
| 1c | 100 | 68 | 70 | 67 | 65 | 70 | 64 | 61 | 61 | ||
| 2a | 100 | 82 | 77 | 67 | 67 | 66 | 66 | 68 | |||
| 2b | 100 | 81 | 64 | 69 | 65 | 67 | 66 | ||||
| 2c | 100 | 64 | 65 | 65 | 66 | 65 | |||||
| 3a | 100 | 79 | 65 | 67 | 64 | ||||||
| 3b | 100 | 66 | 68 | 61 | |||||||
| 4a | 100 | 66 | 66 | ||||||||
| 5a | 100 | 68 | |||||||||
| 6a | 100 |
Som andre RNA-virus saknar HCV eit korrekturlesarsystem (proof reading system) og muterar difor lett. Innanfor kvar subgenotype kan ein finna fleire nukleotidvariasjonar som kan sirkulera i eitt og same individ, så kalla kvasispesies. I viss mon, men truleg ikkje alltid, er dette eit «darwinistisk» resultat av at virus med hjelp av nye mutasjonar (escape mutants) freistar å unngå eit pågåande immunforsvar.[2] [3]
Epidemiologiologisk utvikling[endre | endre wikiteksten]
Allment[endre | endre wikiteksten]
Frå ulike hepatitt C-utbrot med kjende infiseringstidspunkt har det vori mogeleg å rekna fram mutasjonsraten og ei såkalla «molekylær klokke» for utviklinga av hepatitt C-virus. Dei ulike genotypane og subgenotypane har ulik geografisk distribusjon. Ved å jamføra mutasjonsraten med oppstilte fylogenetiske stamtre og kjend geografisk utbreiing av ulike geno- og subgenotypar har ein med statistiske metodar komi fram til teoriar om historisk opphav og epidemiologi når det gjeld HCV. [8] Sekvensskilnaden mellom dei ulike HCV-genotypane kunne tyda på at dei oppstod for mellom 500 og 2000 år sidan. Etter nokre hundre år med endemisk infeksjon i visse geografiske område har dei ulike genotypane vorti spalta i subgenotypar, og truleg har nokre utav desse fyrst på seinare tid vorti spreidde til andre regionar. I endemiske område finn ein difor store skilnader mellom dei ulike HCV-linene. Slike virusstammar vert helst isolerte frå menneske som bur i såvorne område eller har emigrert derifrå.
Det rett så avgrensa talet på subgenotypar i Europa og Nord-Amerika kan tyda på at virus har spreidd seg hit i heller sein tid, truleg frå område der HCV lenge har vori endemisk og hatt tid til å danna talrike subgenotypar. Teoretisk kan det sjå ut som om dei globale genotypane 1, 2 og 3 oppstod for om lag 100 år sidan. Fyrst på 1900-talet, framfor alt etter 1940, vart dei spreidde over heile verda på nye og effektive smittevegar. [9] [10] Resultatet av slike ekstrapoleringar står i viss kontrast till den store utbreiinga som mange utav desse geno- og subgenotypane har fått, så utviklinga har truleg teki lengre tid enn det dei teoretiske utrekningane skulle tyda på. [2]
Ulike genotypar[endre | endre wikiteksten]
Genotype 1
Subgenotypane 1a og 1b (HCV 1a og 1b) er dei vanlegaste typane i Europa, Nord-Amerika og Japan og står globalt for 60 % av alle HCV-infeksjonar. I Europa og Nord-Amerika finn ein HCV 1a fyrst og fremst hjå unge individ med missbruk. HCV 1b er vanlegare hjå eldre personar med blodtransfusjon i anamnesen. Det ser ut som om overføring av genotype 1, framfor alt subgenotypen HCV 1b tok fart på 1940- eller 1950-talet, truleg i samband med smitteførande blodtransfusjonar og blodprodukt, hemodialyse og usteril medisinsk injeksjonsbehandling. I Japan står til dømes typen HCV 1b for over 70 % av tilfella. Mange utav desse stammane ser ut til å ha komi frå USA, kan henda ved import av blod og blodprodukt.
Effektive serologiske screening-/sældingtestar for HCV-smitte har gjort intravenøs misbruk til den viktigaste smittevegen. Både i Europa, Nord-Amerika og Australia finn vi no høgast seroprevalens hjå misbrukarar. «Misbrukarhepatitt» har sidan vorti spreidd frå industri- till utviklingsland. I 1970-åra byrja HCV 1a til dømes å auka kraftig i Vietnam. I sør, der intravenøs misbruk vart vanleg på 1960-talet i samband med at Vietnamkrigen byrja, finst det i dag mange fleire HCV-berarar enn i nord der slik misbruk fyrst vart vanleg etter at krigen tok slutt. I Sentral-Afrika har epidemiologien hatt ei anna utvikling. Her er genotype 1 (saman med genotype 4) dominerande. Desse genotypane er i sin tur spalta i mange ulike subgenotypar og er i dette området truleg «gamle» infeksjonar som har vori endemiske i lang tid. [2] [10] [11] [12]
Genotype 2
HCV 2 er òg ein global genotype, men han er ikkje like vanleg som HCV 1. Subgenotypane HCV 2a og 2b er framfor alt ikkje uvanlege i Europa, Nord-Amerika og Japan. For HCV 2 gjeld det same som for HCV 1; smitteoverføringa ser ut til å ha teki fart på 1940- og 1950-talet med blod, blodprodukt og usterilt, medisinsk fleirgångsutstyr. HCV 2 dominerer i Vest-Afrika, men her tyder oppspalting i mange ulike subgenotypar på ei anna epidemiologisk utvikling. Truleg er HCV 2 ein «gamal», endemisk genotype i vestafrikanske land. [2]
Genotype 3
Subgenotypen HCV 3a gav i 1960- og 1970-åra ein epidemi der fyrst og fremst yngre, intravenøse misbrukarar vart smitta. HCV 3a vart då prevalent i land der misbruk er heller vanleg og har mellom anna både i Europa, Nord- og Sør-Amerika vorti den viktigaste årsaka til «misbrukarhepatitt». Denne subgenotypen er òg dominerande i den norske misbrukarpopulasjonen. [13] Derimot ser ein ikkje HCV 3a så ofte i Japan og afrikanske land der intravenøs misbruk ikkje er eit like stort problem. Av di ulike subgenotypar av HCV 3 er særs vanlege i Aust-Asia, er det viss mistanke om at HCV 3a er spreidd derifrå, kan henda frå land på det nordindiske subkontinentet. [14] [15]
Genotype 4
Globalt er HCV 4 årsak til om lag 20 % av all kronisk hepatitt C. I Sentral-Afrika er ulike subgenotypar utav HCV 4 (saman med HCV 1) dominerande. I dette området er både HCV 1 og HCV 4 skifta i mange ulike subgenotypar og er her truleg «gamle», endemiske genotypar. I Midtausten er HCV 4 årsak til meir enn 80 % av alle heptittilfelle. Med over 15 % av blodgjevarane positive for anti-HCV har Egypt dei høgaste prevalenstala i heile verda. [2] [3] Enda om HCV 4 er årsak til bortimot 90 %, syner denne subgenotypen ikkje så mange sekvensvariasjonar i Egypt som til dømes i Sentral-Afrika. Det epidemiologiske mønsteret ser såleis ut til å vera annleis. Truleg har HCV-smitte vorti spreidd i heller sein tid frå same eller virologisk nærskylde smittekjelder. Epidemiologisk og molekylærbiologisk analyse talar for at HCV 4a-epidemien i Egypt byrja med at kontaminert medisinsk utstyr vart nytta ved parenteral behandling av schistosomiasis føre midten av 1960-talet då medisinsk eingongsutstyr vart vanlegare. På grunn av smittsame blodtransfusjonar og visse ritar har epidemien seinare gått vidare for «eigen maskin». [16]
Genotype 5
HCV 5 finst mest berre i Sør-Afrika.
Genotype 6
Denne genotypen finst så godt som berre i Søraust-Asia, mellom anna i Hongkong og Vietnam der han (saman med HCV 3) er dominerande. HCV 6 har stor sekvensspreiing, viker av frå andre genotypar og er (saman med HCV 3) truleg eit «gamalt», «søraustasiatisk» virus. Talet på infiserte personar ser ut til å ha vori heller konstant fram til omkring 1900, då det tok til å auke dramatisk. Ulike virusstammar som ikkje ser ut til å ha samband med kvarandre vart då dominerande i ulike område der dei årsaka mange lokale epidemiar.
Utpå 1980-talet vart tilvekstkurva for HCV 3 flatare. Tidsmessig ser dette ut til å ha samband med betre hepatitt C-diagnostikk, fyrst og fremst i samband med blodoverføring. [2] [10]
Replikasjon[endre | endre wikiteksten]
På naturleg veg infiserer HCV berre menneske; i eksperiment dessutan sjimpansar. Målorganet ved infeksjon og replikasjon er fyrst og fremst hepatocyttar i levra. Dinest kan HCV replikerast i dendritiske celler og i lymfatiske B-celler, noko som kan henda er viktig for dei immunologiske komplikasjonane ein kan sjå i samband med kronisk hepatitt C. [17]
Ved infeksjon vert virus fyrst festa til målcella. Dette er ein interaksjon mellom virus og fleire typar utav cellulære ytemolekyl som er avgjerande for vevstropismen og dermed for utvalet av dei celletypane som kan infiserast. Ei spesiesvariabel, ekstracellulær slynge (sams for menneske og sjimpansar) utav det humane celleproteinet CD81 fungerer som ko-reseptor når HCV-glykoproteinet E2 vert festa til eit dobbelt lipidlag i målcella. Som resultat utav ein fusjonsprosess mellom virale protein og cellulært membran kjem nukleokapsidet inn i cytoplasmaet i vertcella, truleg ved innposing (endocytose). Her vert den positivt lada RNA-strengen i genomet sleppt ut frå viruskapsidet og inn i cytosolen (det flytande celleinnhaldet) der translasjon og replikasjon går for seg. Ved replikasjonen tener den positive RNA-strengen fyrst som modell for framstilling av ein tilsvarande negativ streng. Denne er i sin tur mellombels naudsynt som mønster for transkripsjon av 5 – 10 gonger så mange positve RNA-strengar. Dei positive strengane vert sidan nytta som bodberar-RNA (mRNA) ved translasjon og syntese av eit mellombels naudsynt polyprotein på drygt 3000 aminosyrer. Virale og cellulære proteaser kløyver sidan dette til ulike protein for replikasjon og oppbygging av nye, ferdige viruspartiklar som skal sleppast fri. [1] [2] [18]
Stabilitet[endre | endre wikiteksten]
Både etiske innvendingar, skort på sjimpansar til dyremodellar og uløyste problem med isolering i cellekultur har tidlegare mellom anna gjort det vanskeleg å skaffa seg nokon god oppfattning om kor lenge HCV kan vera smittefarleg. Enda om laboratorieresultat ikkje bør overtolkast, kan moderne isolerings- og visualiseringsteknikk no i alle fall gjeva visse haldepunkt når nosokomial HCV-smitte kan førebyggjast. HCV ser ut til å klara seg bra i normal omgjevnadstemperatur. I væske, og kan henda i plasma, ser HCV ut til å vera smittsamt i 5 månader ved 4˚C. I kulturmedium er virus truleg smittsamt i så mykje som 16 dagar ved 37˚C, men berre i 4 min. ved 65˚C. HCV er kjensleg for ultrafiolett stråling i 2 minut. Alkoholar som etanol, 1- og 2-propanol og antiseptiske middel som glutaraldehyd og formaldehyd ser òg ut til å ha effekt. [19] [20]
Kjelder[endre | endre wikiteksten]
- ↑ 1,0 1,1 1,2 Chevaliez S, Pawlotsky JM (2006) «HCV Genome and Life Cycle» - i: Hepatitis C Viruses: Genomes and Molecular Biology, kap. 1 (red. Tan, S-L), s 5–47 - Norfolk (UK), Horizon Bioscience. PMID: 21250393. ISBN-10: 1-904933-20-3. [1] (pdf)
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 2,7 Simmonds P (2004) «Genetic diversity and evolution of hepatitis C virus – 15 years on» - J Gen Virol., vol. 85 (Pt 11), s. 3173-3188. PMID: 15483230. [2][daud lenkje] (pdf)
- ↑ 3,0 3,1 3,2 3,3 World Health Organization (2002) «Hepatitis C» - WHO/CDS/CSR/LYO/2003.? Hepatitis C, Global Alert and Response (GAR). [3] (pdf)
- ↑ Pécheur EI, Diaz O, Molle J, Icard V, Bonnafous P, Lambert O, André P (2010) «Morphological characterization and fusion properties of triglyceride-rich lipoproteins obtained from cells transduced with hepatitis C virus glycoproteins» - J Biol Chem., vol. 285, nr. 33, s. 25802-25811. PMID:20551330. [4]
- ↑ Lindenbach BD, Evans MJ, Syder AJ, Wölk B, Tellinghuisen TL, Liu CC, Maruyama T, Hynes RO, Burton DR, McKeating JA, Rice CM (2005) «Complete replication of hepatitis C virus in cell culture»- Science, vol. 309, nr. 5734, s. 623-626. PMID:15947137 (samandrag).
- ↑ Simmonds P, Bukh J, Combet C, Deléage G, Enomoto N, Feinstone S, Halfon P, Inchauspé G, Kuiken C, Maertens G, Mizokami M, Murphy DG, Okamoto H, Pawlotsky JM, Penin F, Sablon E, Shin-I T, Stuyver LJ, Thiel HJ, Viazov S, Weiner AJ, Widell A (2005) «Consensus proposals for a unified system of nomenclature of hepatitis C virus genotypes» - Hepatology, vol. 42, r. 4, s. 962-973. PMID: 16149085. [5] (pdf)
- ↑ Zein NN (2000) «Clinical Significance of Hepatitis C Virus Genotypes» - Clin. Microbiol. Rev., vol. 13, nr. 2, s. 223 - 235. PMID: 10755999. [6][daud lenkje] (pdf)
- ↑ Wróbel B, Torres-Puente M, Jiménez N, Bracho MA, García-Robles I, Moya A, González-Candelas F (2006) «Analysis of the overdispersed clock in the short-term evolution of hepatitis C virus: Using the E1/E2 gene sequences to infer infection dates in a single source outbreak» - Mol Biol Evol., vol. 6, s. 1242-1253. PMID: 16585120. [7] (pdf)
- ↑ Smith DB, Pathirana S, Davidson F, Lawlor E, Power J, Yap PL, Simmonds P (1997) «The origin of hepatitis C virus genotypes» - J Gen Virol., vol. 78 (Pt 2), s. 321-328. PMID: 9018053. [8] (pdf)
- ↑ 10,0 10,1 10,2 Pybus OG, Barnes E, Taggart R, Lemey P, Markov PV, Rasachak B, Syhavong B, Phetsouvanah R, Sheridan I, Humphreys IS, Lu L, Newton PN, Klenerman P (2009) «Genetic history of hepatitis C virus in East Asia» - J Virol., vol. 83, nr. 2, s. 1071-1082. PMID: 18971279. [9][daud lenkje] (pdf)
- ↑ Nakano T, Lu L, Liu P, Pybus OG 2004) «Viral gene sequences reveal the variable history of hepatitis C virus infection among countries» - J Infect Dis., vol. 190, nr. 6, s. 1098-1108. PMID: 15319860. [10] (pdf)
- ↑ Magiorkinis G, Magiorkinis E, Paraskevis D, Ho SY, Shapiro B, Pybus OG, Allain JP, Hatzakis A (2009) «The global spread of hepatitis C virus 1a and 1b: a phylodynamic and phylogeographic analysis» - PLoS Med., vol. 6, nr. 12, e1000198. PMID: 20041120. [11] (pdf)
- ↑ Vik IS, Skaug K, Dalgard O, Steen TW, Hoddevik G (2008) «Hepatitt C - et helseproblem også i Norge» - Tidsskr Nor Laegeforen., vol. 128, nr. 5, s. 563-566. PMID: 18311199. [12] (pdf)
- ↑ Pawlotsky JM, Tsakiris L, Roudot-Thoraval F, Pellet C, Stuyver L, Duval J, Dhumeaux D (1995) «Relationship between hepatitis C virus genotypes and sources of infection in patients with chronic hepatitis C» - J Infect Dis., vol. 171, nr. 6, s. 1607-1610. PMID: 7769300 (samandrag).
- ↑ Morice Y, Cantaloube JU-F, Beaucourt S, Barbotte L, De Gendt S, Goncales FL, Butterworth L, Cooksley G, Gish RG, Beaugrand M, Fay F, Fay O, Gonzalez JE, Bringel Martins RM, Dhumeaux D, Vanderborght B, Stuyver L, Sablon E, de Lamballerie X, Pawlotsky J-M (2006) «Molecular epidemiology of hepatitis C virus subtype 3a in injecting users» - J Med Virol., vol. 78, nr. 10, s. 1296–1303. PMID: 16927280 (samandrag).
- ↑ Kamal SM, Nasser IA (2008) «Hepatitis C genotype 4: What we know and what we don't yet know» - Hepatology, vol. 47, nr. 4, s. 1371- 1383. PMID: 18240152. [13] (pdf)
- ↑ Bartenschlager R, Lohmann V (2000) «Replication of hepatitis C virus» - J Gen Virol., vol. 81 (Pt 7), s. 1631-1648. PMID: 10859368. [14][daud lenkje]
- ↑ Zeisel MB, Fofana I, Fafi-Kremer S, Baumert TF (2011) «Hepatitis C virus entry into hepatocytes: molecular mechanisms and targets for antiviral therapies» - J Hepatol., vol. 54, nr. 3, s. 566-576. PMID: 21146244. [15]
- ↑ Ciesek S, Friesland M, Steinmann J, Becker B, Wedemeyer H, Manns MP, Steinmann J, Pietschmann T,Steinmann E (2010) «How Stable Is the Hepatitis C Virus (HCV)? Environmental Stability of HCV and Its Susceptibility to Chemical Biocides» - J Infect Dis., vol. 201, nr. 12, s. 1859 – 1866. PMID: 20441517. [16]
- ↑ Song H, Li J, Shi S, Yan L, Zhuang H, Li K (2010) «Thermal stability and inactivation of hepatitis C virus grown in cell culture» Virol J., vol. 7, nr. 40, s. 1 – 12. PMID: 20167059. [17] (pdf)
