Absorpsjonsband
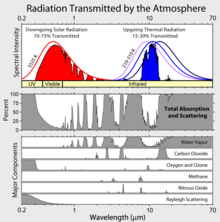
Eit absorpsjonsband er ei rekkje bølgjelengder (eller tilsvarande frekvensar i det elektromagnetiske spekteret) som kan produsere ei særskild omforming av eit stoff. Sidan energirike overgangar kan gå begge vegar, kan absorpsjonsbanda òg fungere som emisjonsband.
Oversyn[endre | endre wikiteksten]
I følgje kvanteteori kan atom og molekyl berre halde på ei viss særskild energimengd, eller berre eksistere med særskilde tilstandar. Derfor kan eit stoff berre endre energi i visse «steg» tilpassa dei tillatne energinivåa dei kan eksistere i. Kvart av desse stega tilsvarar til ei viss energimengd, som kan skildrast som ei bølgjelengd av lys (eller ei spektrallinje). Så når lys frå ein av desse spesifikke bølgjelengdene vekselverkar med eit molekyl, kan denne bølgjelengda verte absorbert, medan andre bølgjelengder passerer forbi. Dette er opphavet til absorpsjonsspeketeret.
Ikkje alle molekyl er heilt like, sjølv molekyla i same stoff. Dei flytte seg forskjellig og vibrere og rotere forskjellig, og ha forskjellige nabomolekyl. På grunn av dette skjer kvar overgang ved litt forskjellige bølgjelengder i forskjellige molekyl, så i staden for ei uendeleg smal absorpsjonslinje i spekteret, ser ein i staden eit band - ei variasjonsbreidde som kvar særskilde overgang kan skje under ved dei riktige tilhøva.
Eigenskapar[endre | endre wikiteksten]
Utforming[endre | endre wikiteksten]
Banda kan ha forskjellig utforming og analysar av desse banda kan gje informasjon om overgangen som har skapt bandet. I mange tilfelle er det nyttig å tenkje seg at eit spektralband er ei enkel gaussisk eller lorentzisk modellform.
Breidde[endre | endre wikiteksten]
Det er mange mekanismar som avgjer breidda til eit absorpsjonsband, som
- Vibrasjonar
- Rotasjonar
- dopplerforbreiing
Forskjellige absorpsjonsband[endre | endre wikiteksten]
Eletroniske overgangar[endre | endre wikiteksten]
Elektroniske overgangar skjer hovudsakleg i energiar som tilsvarar UV-delen og den synlege delen av spekteret. Dei største medverkande faktorane som skapar breiare spektrallinjer i eit absorpsjonsban er fordelinga av vibrasjons- og rotasjonsenergiane til molekyla. I spektroskopi innan gassfasen kan ein skilje finstrukturen som desse faktorane skapar, men i spektroskopi på væskefasen til eit stoff, skapar dei forskjellige molekyla breiare strukturar og glattare band. Elektroniske transisjonsband kan ha ei breidde som varierer frå ti til fleire hundre nanometer.
Vibrasjons- og rotasjonsovergangar[endre | endre wikiteksten]
Vibrasjonsovergangar finn stad i den infraraude delen av spekteret ved bølgjelengder på rundt 1-30 mikrometer.
Rotasjonsovergangar finn òg stad i det infraraude spekteret, men ved lågare energiar enn vibrasjonsovergangar.
Sjå òg[endre | endre wikiteksten]
Kjelder[endre | endre wikiteksten]
- Denne artikkelen bygger på «Absorption band» frå Wikipedia på engelsk, den 14. august 2008.
