Hydrogenbinding
| Kjemiske bindingar |
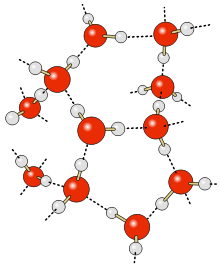
Hydrogenbinding er ei kjemisk binding som eit svakt elektropositivt hydrogenatom i eit molekyl dannar med elektronegative atom som oksygen, nitrogen og fluor i eit anna molekyl. Eit hydrogenatom er svakt elektropositivt når det er kovalent bunde til eit elektronegativt atom. Hydrogenbindinga skjer ved at svakt elektropositive og elektronegative delar av ulike molekyl vert trekte mot kvarandre. Slike bindingar kan òg verka mellom ulike delar av store molekyl. Det er hydrogenbindingar som held basepara i DNA saman.
Hydrogenbindingar førekjem særleg i vatn (H2O). Bindingane er relativt svake, men sidan det er så mange av dei i vatn gjev dei vatnet spesielle fysiske eigenskapar som eit svært høgt kokepunkt, sidan det trengst mykje energi for å bryta desse bindingane mellom molekyla. Den tilsvarande kjemiske sambindinga til grunnstoffet svovel, som ligg under oksygen i periodesystemet – hydrogensulfid (H2S) – har ikkje hydrogenbindingar og er ein gass ved romtemperatur sjølv om han har dobbelt så høg molekylvekt som vatn. Hydrogenbindingar gjev òg vatn høg varmekapasitet, det vil seia at det trengst mykje energi for å varme opp vatn.
Hydrogenbindingar gjev samtidig vatnet spesielle eigenskapar når det frys. Som dei fleste andre material blir tettleiken til vatnet større ved lågare temperatur. Men når vatn blir kjølt ned til nær frysepunktet, fører hydrogenbindingane til at det blir danna ein struktur som faktisk har lågare tettleik fordi vassmolekyla flyttar på seg for å minske energien sin. Dermed vil vatn utvida seg når det frys og is vil flyta i vatn, medan dei fleste andre material krympar og søkk når dei går over til fast form.
